- Process validation follows three stages: IQ, OQ, and PQ.
- Validation is legally required for medical and automotive parts.
- A well-run validation saves more money than it costs within the first production run.
- Cpk values above 1.33 indicate a capable and stable process.
- Start validation during mold design — never after first article approval.
What Is Injection Molding Process Validation?
Литье под давлением process validation1 is defined by the function, constraints, and tradeoffs explained in this section. If you are comparing vendors or planning procurement, our injection molding supplier sourcing guide covers RFQ prep, qualification, and commercial risk checks.
You just got a call from your customer’s quality team. They want to see your validation protocol before they approve the first production run. If you can’t produce documented evidence that your process is under control, the shipment stops. That’s not a hypothetical — it happens every week in medical device and automotive supply chains.
Injection molding process validation is a structured, documented method for proving that your molding process consistently produces parts that meet every specification — dimensional, material, cosmetic, and functional. It’s not a one-time test. It’s evidence that your process holds up run after run, shift after shift.

The core framework is IQ/OQ/PQ — Installation Qualification, Operational Qualification, and Process Qualification2. Each stage builds on the previous one. Skip one, and the whole validation collapses under audit scrutiny.
Here’s the bottom line: validation costs money upfront, but a single rejected lot or customer audit failure costs ten times more. In our experience at ZetarMold, a well-prepared validation protocol pays for itself within the first production run by catching process drift before it creates scrap.
Why Does Process Validation Matter?
Validation matters because inconsistency is invisible until it’s expensive. A part that measures 10.02 mm today and 10.08 mm next week looks fine to the naked eye — but it’s a tolerance failure waiting to happen. Without validation data, you won’t know until the customer’s incoming inspection catches it.
For regulated industries, validation isn’t optional. The FDA requires it under 21 CFR Part 820 for medical devices. IATF 16949 demands it for automotive components. If you’re supplying parts into these markets and you can’t produce validation records, you’re not compliant. Period.
But even if you’re not in a regulated space, validation still pays off. Here’s what we’ve seen on the factory floor at ZetarMold: projects that skip validation typically show 3–5× higher scrap rates in the first three months compared to validated processes. The pattern is consistent — unvalidated processes drift, and nobody notices until the scrap bin fills up.
The financial argument is straightforward. A typical validation for a single-cavity mold runs $3,000–$8,000 depending on complexity. A single rejected shipment of 10,000 parts at $2.50 each costs $25,000 in remakes, plus shipping, plus the trust damage with your customer. The math speaks for itself.
| Validation factor | Key consideration |
|---|---|
| Tooling | Confirm how mold design affects Injection Molding Process Validation: Complete Guide for Engineers. |
| Материал | Check resin behavior, shrinkage, heat, and cosmetic risks. |
| Качество | Ask for inspection evidence before production approval. |
Beyond cost, validation builds customer confidence. When a buyer knows your process is validated with documented Cpk values and proven parameter windows, they trust your production capability. That trust translates into larger orders, longer contracts, and fewer incoming inspection requirements on future shipments. It becomes a competitive advantage, not just a compliance exercise.
“Process validation reduces scrap rates by 60–80% in the first year of production.”Правда
By establishing proven parameter windows before full production, validation catches process drift early. At ZetarMold, validated jobs consistently achieve first-pass yields above 95%, compared to 75–85% for unvalidated processes.
“Process validation is only necessary for medical device manufacturing.”Ложь
While the FDA mandates validation for medical devices, industries like automotive (IATF 16949), aerospace (AS9100), and electronics also require it. Even consumer product companies benefit from validation through reduced defects and warranty claims.
What Are the Three Stages of Process Validation?
The three stages of process validation are the main categories or options explained in this section. The IQ/OQ/PQ framework has been the industry standard since the 1980s. Each stage answers a specific question. IQ asks: is the machine installed correctly? OQ asks: does it work across its operating range? PQ asks: can it produce acceptable parts consistently over time?
Stage 1: Installation Qualification (IQ)
литьё под давлением3 verifies that the equipment is set up exactly as specified. This means checking the machine’s utilities (power, water, air), confirming software versions, verifying calibration certificates, and documenting every connection.
In practice, IQ is a checklist-driven process. You walk through every item on the installation specification and document that it matches reality. Common failures at this stage include incorrect water flow connections (which affect cooling), wrong voltage settings, and missing calibration records on ancillary equipment like dryers and loaders.

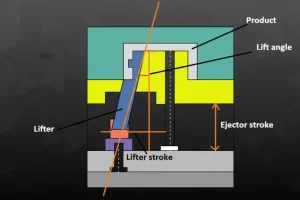
A proper IQ protocol includes: equipment identification (model, serial number, firmware version), utility verification (voltage, water pressure, air pressure), safety system checks (ejector stroke limits, emergency stops), and environmental conditions (temperature, humidity of the molding area). Each item gets a pass/fail result with inspector sign-off.
Don’t underestimate IQ. We’ve seen projects delayed by weeks because someone skipped verifying the thermolator connections and the mold ran with inadequate cooling during OQ. The resulting data was worthless because the process conditions weren’t representative. Always complete IQ before touching the molding machine for any process development work.
Stage 2: Operational Qualification (OQ)
Operational Qualification proves that the process works across its entire intended operating range. This is where you deliberately push parameters to their limits — high and low melt temperatures, fast and slow injection speeds, minimum and maximum packing pressures — to map out the process window.
The output of OQ is a documented process window. You should know, with data, that your part will be acceptable when melt temperature is between 220°C and 250°C, injection speed is 50–80 mm/s, and holding pressure is 800–1200 bar. Every parameter has a proven upper and lower limit.
The most efficient way to run OQ is using a Design of Experiments approach. Instead of testing one variable at a time (which requires hundreds of runs), a fractional factorial DOE can map critical interactions in 16–32 runs. For a typical injection molding process with 4–6 critical parameters, this takes 2–3 days on the machine.
During OQ, document everything. Machine settings, ambient conditions, material lot numbers, cycle times for every shot, and all measurement results. This data becomes your baseline reference for the entire production life of the mold. If quality issues arise two years from now, you’ll need this OQ data to diagnose whether the process has shifted.
One common mistake during OQ is testing parameters in isolation. Melt temperature affects viscosity, which changes injection speed requirements, which shifts packing behavior. If you test melt temperature alone with all other parameters fixed, you miss the interaction effects. That is why DOE matters — it captures these multi-variable relationships in a single experimental design.
Another practical tip: run your OQ on the same material lot you plan to use for PQ. Different resin lots can have viscosity variations of 10 to 15 percent, which shifts the process window enough to invalidate your OQ results. We always confirm material lot consistency before starting any OQ campaign at our Shanghai facility.
Stage 3: Process Qualification (PQ)
Process Qualification is the final proof. You run the process at its nominal settings over multiple consecutive runs — typically three separate production runs on different days, shifts, or operators — and demonstrate that every part meets specification.
PQ is not about finding the process window. That’s OQ’s job. PQ is about proving stability. If you set the machine to the center of your validated window and run 300 parts across three different days, and all 300 pass inspection, you have statistical evidence that your process is stable.
The statistical tool for PQ is capability analysis. You calculate Cpk (process capability index) for every critical dimension. A Cpk of 1.33 means your process fits within the tolerance band with room to spare. Below 1.0 means you’re producing out-of-spec parts regularly. Most automotive OEMs require Cpk ≥ 1.67 for critical dimensions.
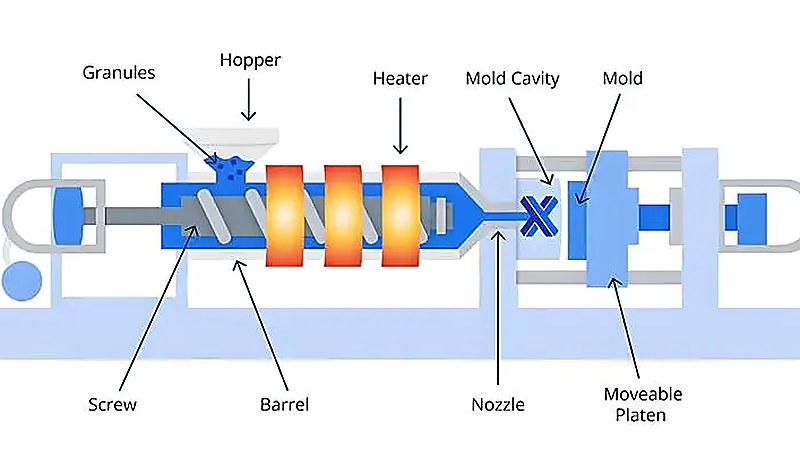
At ZetarMold, we run PQ on our 47 injection molding machines ranging from 90T to 1850T. Our standard protocol requires three consecutive successful runs with Cpk ≥ 1.33 on all critical dimensions before we consider a process validated and ready for production release. Our 8 senior engineers, each with 10+ years of experience, review every PQ package before sign-off.
“A Cpk value of 1.33 means the process produces fewer than 63 defective parts per million.”Правда
Cpk 1.33 corresponds to a 4-sigma process capability, meaning the process mean is at least 4 standard deviations from the nearest specification limit. This translates to approximately 63 ppm defect rate — a widely accepted threshold for capable processes.
“Process Qualification only needs to be done once for each mold.”Ложь
PQ must be repeated whenever there are significant changes: material lot changes, mold modifications, machine relocation, or after extended shutdowns. Revalidation is also triggered if statistical process control data shows the process has drifted from its validated state.
In our Shanghai factory, 47 injection molding machines from 90T to 1850T give us the flexibility to run PQ across a wide range of part sizes and materials. With 20+ years of experience and 8 senior engineers overseeing every validation package, we’ve built a systematic approach that gets your process validated faster and with higher confidence.
How Do You Verify Injection Molded Parts?
Verification is the measurement side of validation. While validation proves the process is capable, verification proves that the actual parts coming off the machine meet specifications. The two work together — validation without verification is just paperwork.
The four core verification methods are dimensional checks, visual inspection, material property testing, and functional testing. Each addresses a different failure mode, and skipping any of them leaves a blind spot in your quality system.
Dimensional verification uses CMM (Coordinate Measuring Machine) for tight-tolerance features and calipers or optical comparators for general dimensions. A proper first-article inspection report covers every dimension on the drawing — not just the ones that look easy to measure.
Visual inspection catches cosmetic defects: flash, sink marks, splay, color variation, and weld lines. In our facility, we use trained inspectors who check every part against an approved visual standard with defined accept/reject criteria. Subjective ‘it looks fine’ judgments don’t survive an audit.
Material testing includes melt flow index (MFI) verification, tensile testing, and hardness measurement. For medical and automotive parts, material certification (Certificate of Analysis from the resin supplier) is required for every lot — not just the first one.
Functional testing confirms the part works in its intended application. This might be a snap-fit engagement force test, a leak test for fluid-handling components, or an electrical continuity test for connector housings. The test method should replicate actual use conditions.
At ZetarMold, our six-step quality control process covers every stage from incoming material inspection (IQC) through final outgoing inspection (OQC). With 10+ QC specialists and a full suite of measurement equipment including CMM, profile projectors, and hardness testers, we provide the verification data that supports your validation package.
What Is the Difference Between Mold Qualification and Process Validation?
The difference between mold qualification and process validation is defined by the function, constraints, and tradeoffs explained in this section. This question comes up in almost every audit. Mold qualification focuses on the tool itself — does the mold produce parts to spec? Process validation is broader — it proves the entire system (machine, mold, material, operator, environment) works together consistently.
You can qualify a mold on a bench-top machine in a lab. But process validation has to happen on the production equipment, in the production environment, with production operators and production materials. That’s the key distinction that many engineers overlook when planning their validation timeline.
In practice, mold qualification is a subset of process validation. You verify the mold first (steel hardness, surface finish, cavity dimensions, ejection system), then validate the process around it. If a part fails, mold qualification tells you whether to fix the tool or adjust the process.
| Аспект | Mold Qualification | Валидация процесса |
|---|---|---|
| Scope | Tool only | Machine + mold + material + environment |
| Когда | After mold build | Before production release |
| Runs needed | T1 samples (50–100 parts) | 3+ consecutive production runs |
| Statistical requirement | Dimensional report | Cpk ≥ 1.33 on critical dims |
| Re-trigger | Mold modification or rework | Material change, machine change, or process drift |
| Ownership | Tool shop / mold maker | Production quality team |
What Parameters Should You Validate?
This section is about parameters should you validate and its impact on cost, quality, timing, or sourcing risk. Not every parameter needs validation. Focus on the ones that directly affect part quality. Over-validating wastes machine time; under-validating creates risk. The trick is knowing which parameters are critical for your specific part geometry and material.
The critical parameters for most injection molding processes are: melt temperature, injection speed, holding pressure, holding time, cooling time, and mold temperature. These six parameters control 90% of part quality outcomes across most applications.
Here’s a practical approach we use at ZetarMold: run a screening DOE with these six parameters at two levels each. The DOE results tell you which parameters are statistically significant for your specific part. Typically, 2–3 parameters dominate quality. Those are the ones you validate rigorously. The rest get standard operating ranges.
For precision parts with tight tolerances (±0.05 mm or tighter), packing pressure and melt temperature are almost always the dominant factors. For thin-wall parts, injection speed and mold temperature take over. For structural parts with thick sections, cooling time and holding pressure are critical.
Don’t forget the secondary parameters. Barrel temperature profile (not just the set point, but the actual front/center/rear zone temperatures), back pressure, screw speed, and decompression distance all affect consistency. Document them during validation, even if you don’t statistically test them.
Also validate your auxiliary systems. Dryer performance (dew point and residence time) affects material viscosity, which shifts every parameter downstream. Mold temperature controllers need stable output — a thermolator that fluctuates ±5°C will create dimensional variation that no amount of machine parameter tuning can compensate for.
How Long Does Process Validation Take?
This section is about long does process validation take and its impact on cost, quality, timing, or sourcing risk. For a typical single-cavity mold with moderate complexity, the full IQ/OQ/PQ cycle takes 5–10 business days. IQ is usually 1 day (equipment verification and documentation). OQ takes 2–4 days depending on the number of parameters and DOE runs. PQ takes 2–3 days for the three consecutive production runs plus measurement and data analysis.
Multi-cavity molds take longer because you need to validate each cavity individually and demonstrate cavity-to-cavity consistency. An 8-cavity mold can take 15–20 days for full validation. The measurement time is the bottleneck — CMM inspection of all critical dimensions across multiple cavities and multiple runs adds up quickly.
Here’s a rule of thumb from our 20+ years of operation at ZetarMold: plan for validation to take 10–15% of the total mold build timeline. If your mold takes 8 weeks to build, expect 4–6 days of validation. If you’re rushing, you can compress it, but you’ll sacrifice statistical confidence.
The biggest time risk is measurement. If your CMM lab is backlogged, PQ data can take an extra 2–3 days to process. Plan measurement capacity in advance, especially if you’re validating multiple parts simultaneously. Our 120+ production team and dedicated QC staff help us turn around validation packages efficiently.
What Documentation Do You Need?
The validation package is the final deliverable. Without proper documentation, validation didn’t happen — at least not in the eyes of an auditor. Here’s what a complete package includes.
Сайт проектирование пресс-форм для литья под давлением validation master plan outlines the scope, responsibilities, acceptance criteria, and schedule. Think of it as the project plan for validation. It should be approved before any validation work begins.
IQ protocol and report documents every verified installation item with pass/fail results, signatures, and dates. OQ protocol and report includes the DOE design, parameter ranges tested, and resulting process windows with supporting data. PQ protocol and report shows the consecutive run results with capability analysis (Cpk calculations) for all critical dimensions.
Supporting documents include: first article inspection reports, material certificates of analysis, equipment calibration records, operator training records, and any deviation reports with root cause analysis. A well-organized validation package for a moderately complex part runs 40–80 pages.
Keep your validation records accessible. During audits, you’ll need to retrieve specific run data, measurement results, and sign-off sheets quickly. A well-indexed digital archive saves hours of audit preparation time. We maintain complete validation records for every production mold at our Shanghai facility, organized by part number and revision level.
When Should You Revalidate?
This section is about revalidate and its impact on cost, quality, timing, or sourcing risk. Validation isn’t permanent. Changes to the process, equipment, material, or environment can invalidate your previous results. The key is knowing when full revalidation is required versus when a simple verification is sufficient.
Full revalidation (IQ + OQ + PQ) is required when: the mold is moved to a different machine, there’s a major mold modification (adding a cavity, changing gate location, replacing core inserts), or the material grade changes. Partial revalidation (OQ + PQ) may be sufficient for minor changes like adjusting process parameters within the validated range.
Ежегодные пересмотры валидации являются стандартной практикой в регулируемых отраслях. Даже если ничего не изменилось, вы анализируете данные SPC за прошедший год, подтверждаете, что значения Cpk всё ещё выше порогового уровня, и документируете этот пересмотр. Это иногда называется «продолжающейся проверкой процесса» и требуется в соответствии с руководством FDA.
На нашем объекте в Шанхае наши 8 старших инженеров ежемесячно проверяют статус валидации. Любой процесс, показывающий снижение Cpk ниже 1,33 по критическим размерам, запускает автоматическое расследование и потенциальную повторную валидацию. Этот проактивный подход предотвращает утечки качества до того, как они достигнут клиента.
Часто задаваемые вопросы
Что такое валидация процесса литья под давлением?
Валидация процесса литья под давлением — это документированная процедура, основанная на доказательствах, которая подтверждает, что ваш процесс формования стабильно производит детали, соответствующие всем спецификациям по размерным, материальным, косметическим и функциональным критериям. Она следует трём определённым этапам: Квалификация установки (IQ), Квалификация эксплуатации (OQ) и Квалификация процесса (PQ). Цель — установить документированную статистическую уверенность в том, что процесс каждый раз работает в пределах заданных параметров, независимо от вариаций оператора, сменных изменений или различий в партиях материала. Валидация требуется регулирующими органами, включая FDA и IATF, для критических отраслей.
Требуется ли валидация процесса для всех деталей, изготовленных литьём под давлением?
Валидация процесса является юридически обязательной для медицинских устройств согласно FDA 21 CFR Part 820, автомобильных компонентов согласно IATF 16949 и аэрокосмических деталей согласно AS9100. Для потребительских товаров и общих промышленных применений она не является юридически обязательной, но настоятельно рекомендуется специалистами по качеству. Причина проста: стоимость типичного протокола валидации (от 5 000 до 15 000 долларов для одногнездной формы) намного меньше, чем стоимость единичного упущения в качестве, отзыва продукции или отклоненной поставки. Даже нерегулируемые производители получают выгоду от сокращения гарантийных претензий, снижения уровня брака и повышения доверия клиентов, когда их процессы должным образом валидированы с задокументированными диапазонами параметров.
В чём разница между IQ, OQ и PQ?
IQ (Квалификация установки) проверяет, что всё оборудование было правильно установлено, включая подключение коммуникаций, записи калибровки и версии программного обеспечения. Она отвечает на вопрос: правильно ли настроена машина? OQ (Квалификация эксплуатации) демонстрирует, что процесс работает в пределах своего предполагаемого рабочего диапазона, путём тестирования пределов параметров с использованием методологии Планирования эксперимента. Она отвечает: работает ли процесс на своих крайних значениях? PQ (Квалификация процесса) доказывает стабильное качество производства в течение нескольких последовательных запусков с анализом статистической способности с использованием расчётов Cpk. Она отвечает: можем ли мы доверять этому процессу каждый раз? Каждый этап основывается на предыдущем и должен быть выполнен последовательно.
Сколько деталей необходимо для валидации процесса?
Не существует единого фиксированного числа, обязательного для всех отраслей, но устоявшаяся практика требует трех отдельных производственных запусков, как правило, в разные смены, дни или с участием разных операторов, со статистически значимыми размерами выборки на каждый запуск. Для квалификации процесса типичные размеры выборки составляют от 30 до 50 деталей на запуск для анализа размеров, что дает от 90 до 150 общих точек данных на каждый критический размер для расчета Cpk. Многогнездные формы требуют репрезентативных образцов из каждой полости в каждом запуске, чтобы продемонстрировать согласованность между полостями. Производители медицинских устройств могут требовать больших размеров выборки в зависимости от класса риска детали и уровня статистической достоверности, указанного в протоколе валидации.
Какое значение Cpk приемлемо для валидированных процессов?
Cpk больше или равен 1,33 — это минимально принятый порог для способного процесса в большинстве производственных контекстов. Это значение соответствует примерно 63 дефектам на миллион возможностей, что означает, что среднее значение процесса находится на расстоянии не менее четырёх стандартных отклонений от ближайшего предела спецификации. Автомобильные OEM-производители часто требуют Cpk больше или равен 1,67 для критических размеров безопасности, что соответствует примерно 0,6 дефектам на миллион. Компании по производству медицинских устройств обычно стремятся к Cpk больше или равен 1,33, но могут требовать более высоких значений для критически важных для пациента характеристик. Любое значение Cpk ниже 1,0 указывает на то, что процесс регулярно производит детали вне спецификации и требует немедленных корректирующих действий и потенциальной повторной валидации до продолжения производства.
Как часто следует повторять валидацию процесса литья под давлением?
Полная повторная валидация, охватывающая все три этапа (IQ, OQ и PQ), требуется всякий раз, когда процесс значительно изменяется, включая перемещение формы на другую машину, серьезные модификации формы, такие как добавление полостей или изменение мест расположения литников, смену марок материала или переезд на другое предприятие. Для регулируемых отраслей, включая медицинские устройства и автомобилестроение, требуются ежегодные обзоры постоянной верификации процесса, даже если никаких изменений не произошло. Во время этих обзоров команды по качеству изучают данные SPC за последние двенадцать месяцев и подтверждают, что значения Cpk остаются выше порогового уровня по всем критическим размерам. Если мониторинг SPC обнаруживает снижение Cpk ниже 1,33 по любому критическому размеру в любой момент, повторная валидация должна быть запущена немедленно, а не ждать запланированного ежегодного обзора.
Какова роль DOE в валидации литья под давлением?
Планирование эксперимента (DOE) играет критическую роль на этапе Квалификации эксплуатации, эффективно отображая взаимосвязь между параметрами процесса и результатами качества деталей. Вместо тестирования одного фактора за раз, что потребовало бы сотен экспериментальных запусков, DOE изменяет несколько факторов одновременно в соответствии со структурированным статистическим планом. Этот подход выявляет взаимодействия параметров, которые тестирование одного фактора полностью упускает. Типичный дробный факторный DOE с четырьмя-шестью параметрами процесса требует всего 16–32 запусков, чтобы определить, какие факторы статистически значимы, и установить проверенные окна параметров с документированными верхними и нижними пределами для каждой критической переменной.
Можно ли провести валидацию процесса на прототипной форме?
Валидацию процесса технически можно выполнить на прототипной форме, но результаты валидации применимы только к этой конкретной комбинации формы, машины и материала в точных условиях тестирования. Если вы проводите валидацию на прототипной мягкой форме, а затем переходите на производственную твердую форму, всю валидацию необходимо повторить, поскольку производственная форма будет иметь другую компоновку каналов охлаждения, конструкцию литников, количество полостей, отделку поверхности и типы стали. Все эти различия фундаментально влияют на поведение процесса, что означает, что исходные данные валидации не могут быть перенесены на новый инструмент. По этой причине большинство инженеров по качеству рекомендуют проводить валидацию непосредственно на производственной форме, чтобы избежать дублирования усилий и затрат.
-
валидация процесса: Валидация процесса относится к систематической процедуре сбора и оценки данных на этапах проектирования и производства для установления документированных доказательств того, что производственный процесс, работающий в установленных параметрах, стабильно производит продукт, соответствующий его предопределённым спецификациям и качественным характеристикам. ↩
-
Квалификация процесса: Квалификация процесса (PQ) — это заключительный этап валидации процесса, который демонстрирует, что производственный процесс стабильно производит продукцию, соответствующую заранее установленным спецификациям, во время фактических производственных запусков. ↩
-
injection molding: injection molding refers to is the production process that melts plastic, injects it into a mold cavity, cools the part, and repeats the cycle for stable volume manufacturing. ↩